Mesures de la Confédération pour réduire les coûts de la santé et promouvoir les génériques et les biosimilaires – résumées pour vous
- Les médicaments soumis à ordonnance (LS) dont le prix d’achat/prix de fabrique (PF) est inférieur à 15 CHF seront plus chers au prix public et les médicaments dont le prix d’achat/ prix de fabrique (PF) est supérieur à 15 CHF seront moins chers.
- Même part relative à la distribution pour les originaux/génériques et pour les biologiques/ biosimilaires
- En choisissant des génériques et des biosimilaires
- avec un prix de fabrique (PF) plus avantageux -> moins d’immobilisation de capital
- moins de charges administratives grâce à la suppression de l’obligation de documentation
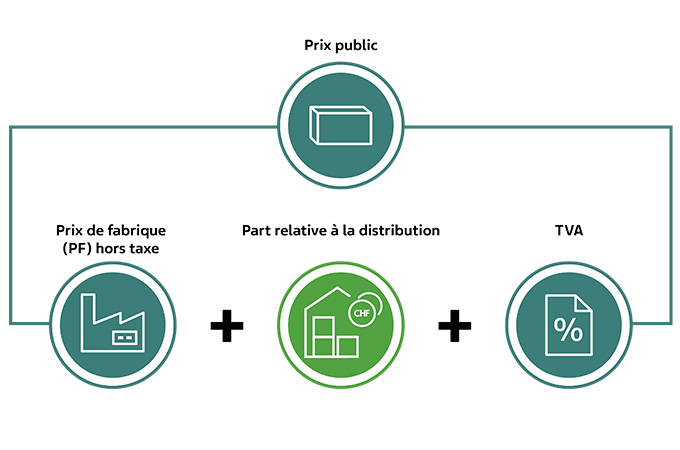
Les détails accompagnés d’exemples de calcul
Au 1er juillet 2024, l’Office fédéral de la santé publique (OFSP) mettra
en œuvre un nouveau modèle de calcul du prix public. Cette mesure permettra de limiter les coûts de la santé et d’encourager la prescription
de génériques et de biosimilaires. Les prix publics sont donc amenés à
changer.
Le changement du prix public repose sur deux ajustements de la part relative à la distribution:
1) Le modèle de calcul de la part relative à la distribution pour les médicaments soumis à ordonnance sera adapté
2) Une part relative à la distribution uniforme sera introduite pour les médicaments ayant le même principe actif
1) Modèle de calcul de la part relative à la distribution des médicaments soumis à ordonnance (OPAS art. 38 al. 1 et 2)
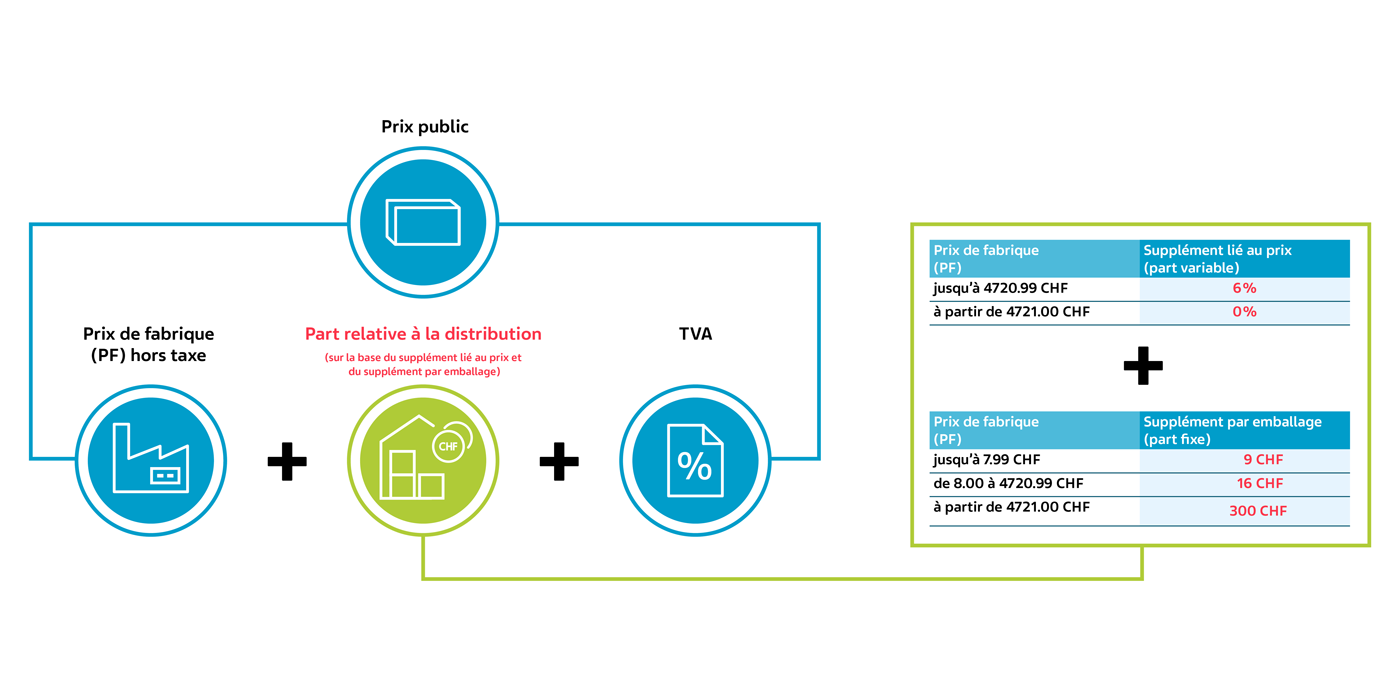
Le calcul de la part relative à la distribution se compose d’un supplément lié au prix (part variable) et d’un supplément par emballage (part fixe).


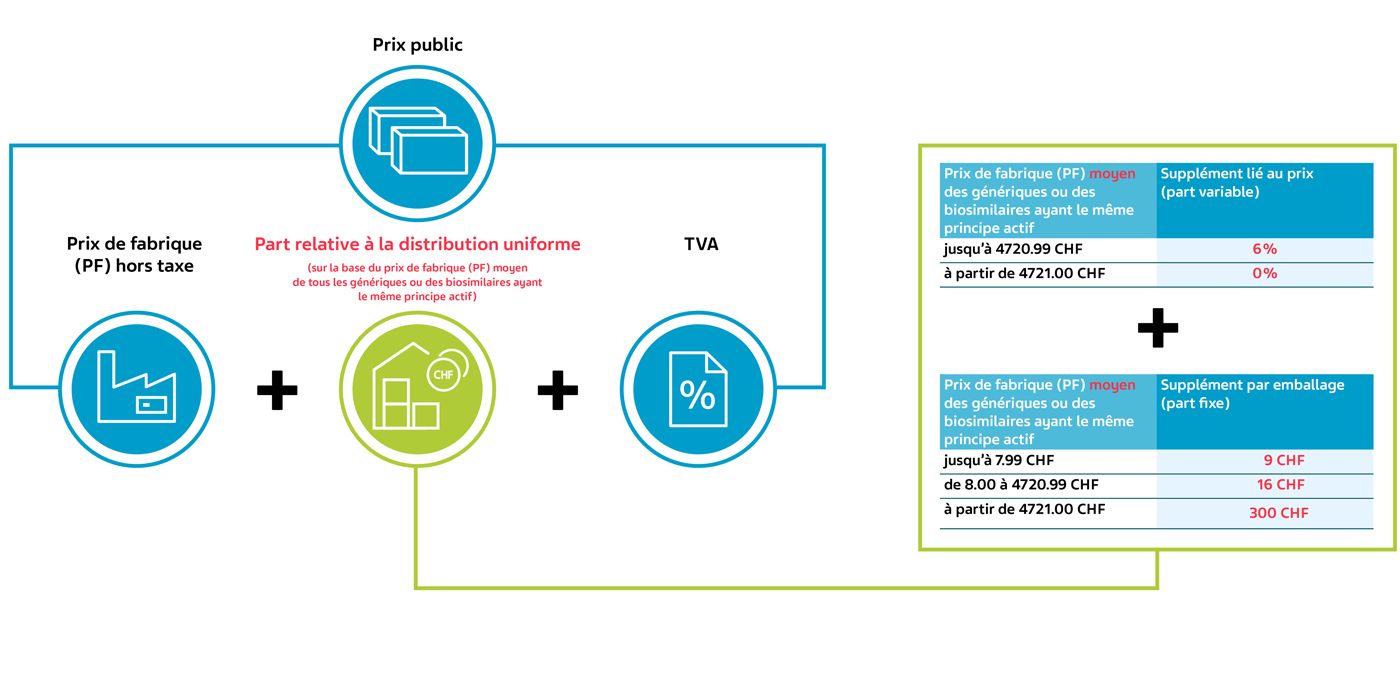
2) Part relative à la distribution uniforme (OPAS art. 38 al. 4)
Désormais, la part relative à la distribution des médicaments ayant le même principe actif est fixée sur la base du prix de fabrique (FP) moyen des génériques ou des biosimilaires.
Nouveau à partir du 1er juillet 2024 – pour les médicaments ayant le même principe actif
(pour les médicaments LS de la liste A, B et D)
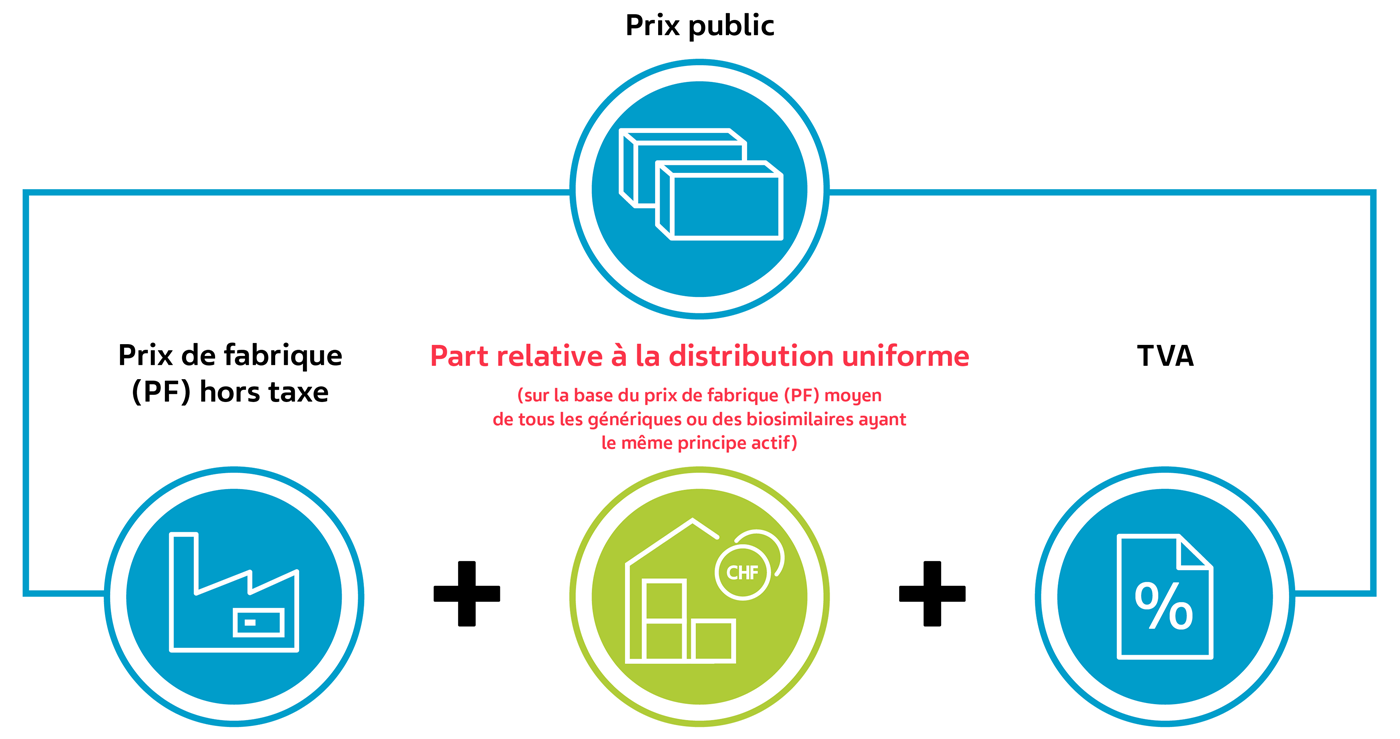
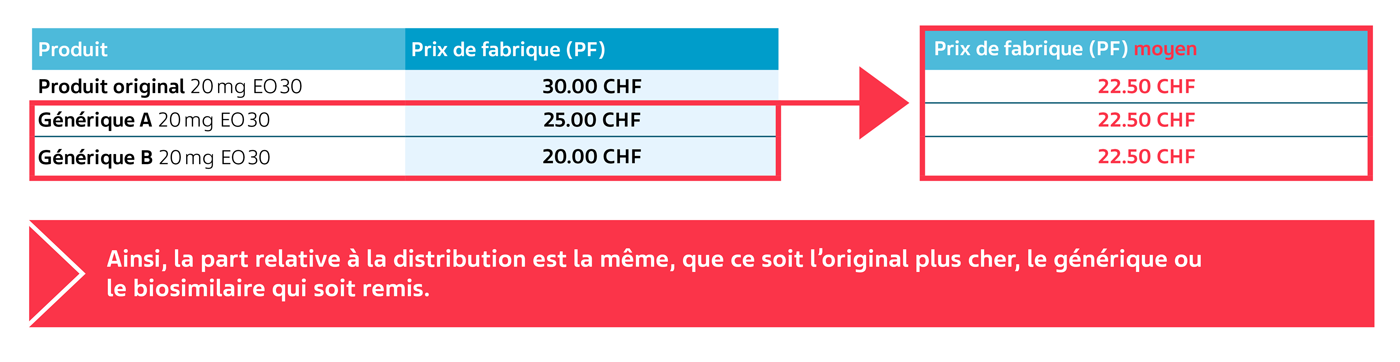
Calcul du prix de fabrique (PF) moyen à partir d’un exemple fictif:
Le prix de fabrique (PF) moyen des génériques A et B est de 22.50 CHF et sert de valeur de départ pour le calcul de la part relative à la distribution pour tous les médicaments de la LS ayant le même principe actif.
Exemples de calcul
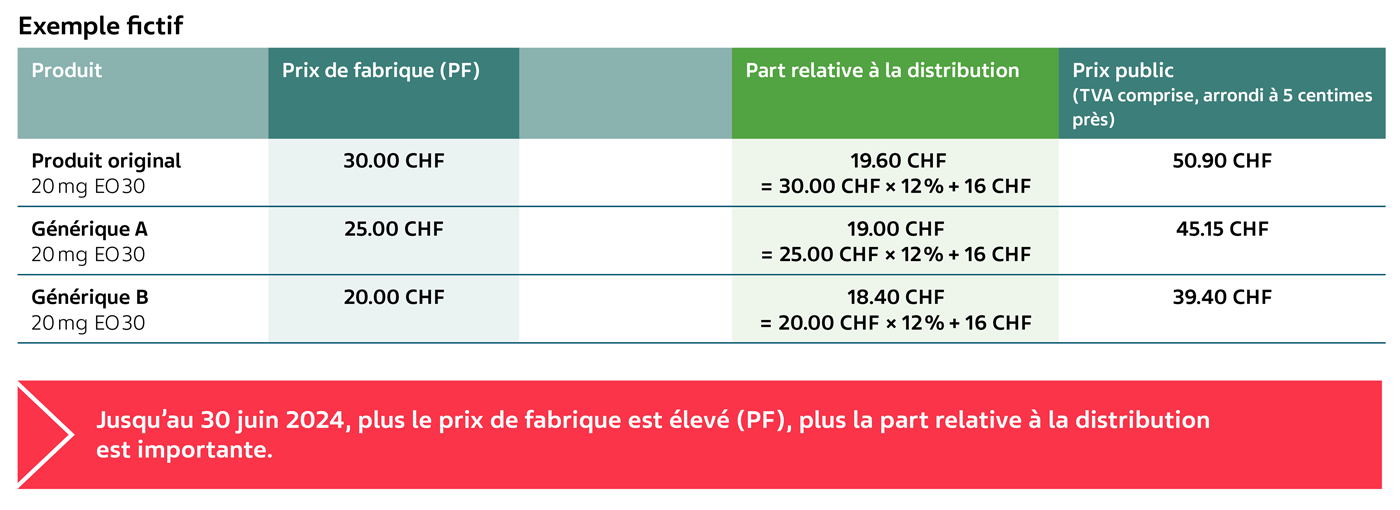
Jusqu’au 30 juin 2024 – pour les médicaments de la liste A/B
Calcul du prix public des médicaments de la liste des médicaments LS, liste A/B jusqu’au 30 juin 2024 à l’aide d’un exemple fictif (OPAS art. 38 al. 1 et 2):

Nouveau à partir du 1er juillet 2024 – pour les médicaments de la liste A/B
Nouveau calcul du prix public à partir du 1er juillet 2024 à l’aide d’un exemple fictif (OPAS art. 38 al. 1 et 2):

Nouveau à partir du 1er juillet 2024 – pour les médicaments de la liste A/B
Nouveau calcul du prix public à partir du 1er juillet 2024 à l’aide d’un exemple fictif (OPAS art. 38 al. 1 et 2):
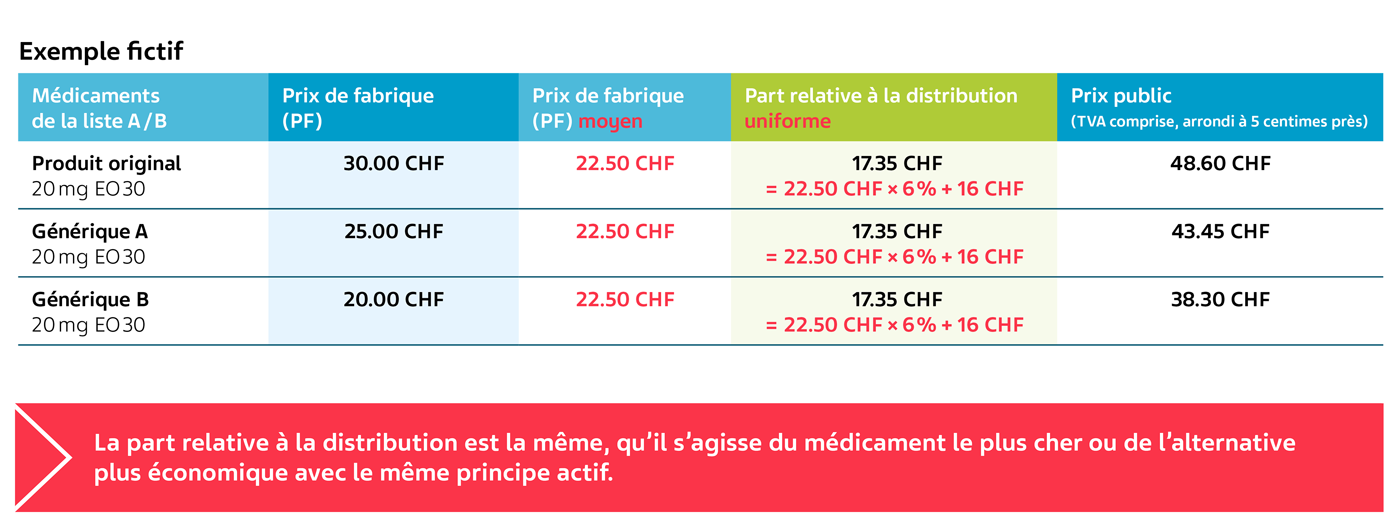
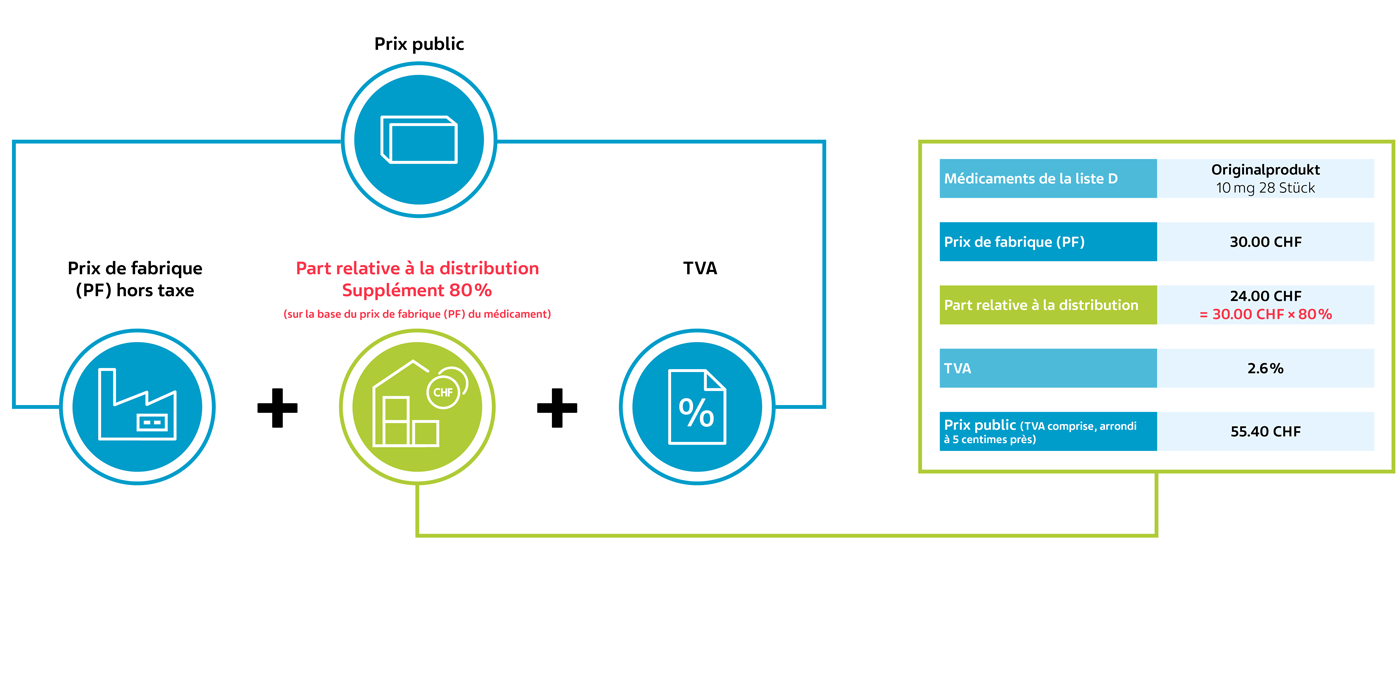
Pour les préparations de la liste D de la LS, le calcul de la part relative à la distribution reste le même pour autant qu’aucun médicament moins cher et ayant le même principe actif ne soit répertorié.
Calcul du prix public pour les médicaments de la LS de la liste D (OPAS art. 38, al. 1 et 2):
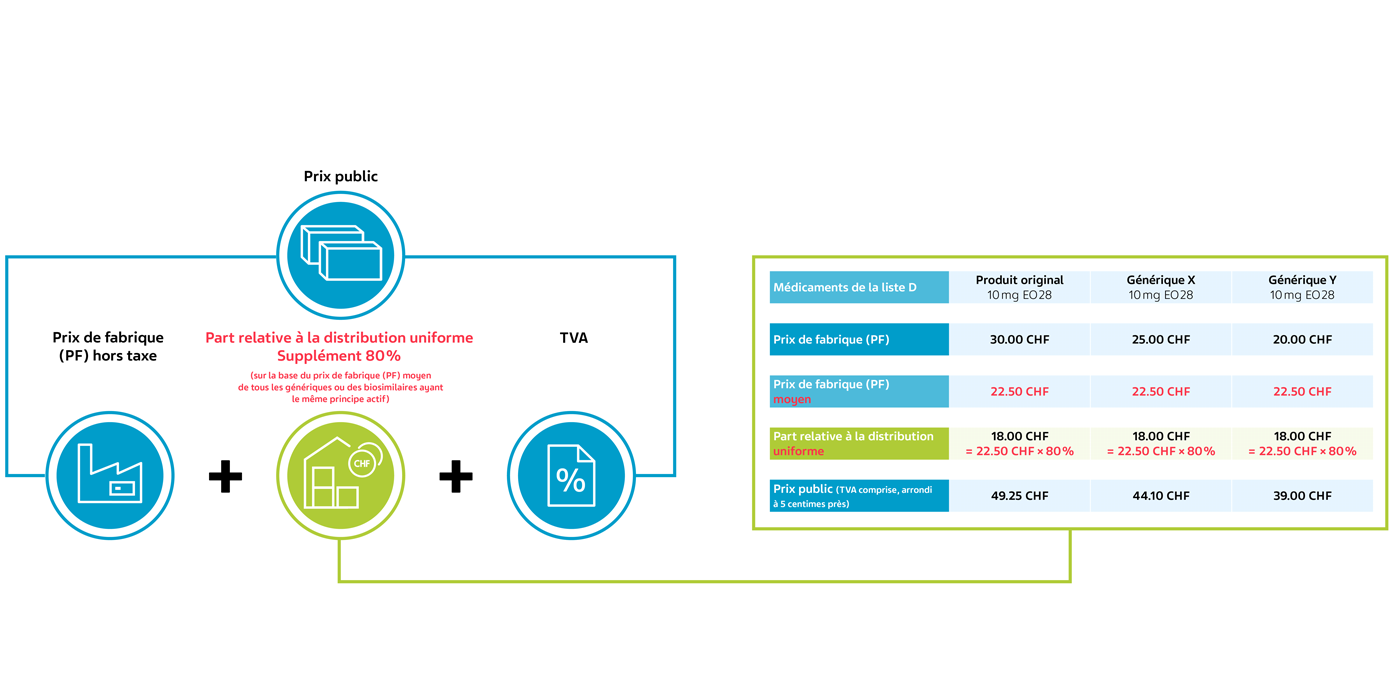
Nouveau à partir du 1er juillet 2024 – pour les médicaments de la liste D ayant le même principe actif
Calcul du prix public des médicaments de la liste D ayant le même principe actif valable à partir du 1er juillet 2024 à l’aide d’un exemple fictif (OPAS art. 38, al. 1 et 2):
Les mesures de la Confédération visant à réduire les coûts des soins de santé et à promouvoir les génériques et les biosimilaires sont entrées en vigueur dès le 1er janvier 2024. Ces changements affectent les médicaments figurant sur la liste des spécialités. Les changements les plus importants par rapport à ces bases juridiques1 sont les suivants:
Quote-part augmentée (art. 38a OPAS et art. 140a al. 2 OAMal)
- La quote-part a doublé, passant de 20% à 40%. Cette règle s’applique désormais également aux médicaments issus de la biotechnologie.
- Les produits dont la quote-part a été augmentée sont signalés par une croix rouge dans la colonne QP de la liste des spécialités (www.spezialitätenliste.ch).
Exemple comparatif de quote-part augmentée:


- Pour les produits avec une quote-part plus élevée, ce ne sont pas 40% mais 25% seulement qui sont pris en compte dans la quote-part de 700.– CHF.
- Pour les produits avec une quote-part de 10%, la totalité des 10% est prise en compte dans les 700.– CHF
En choisissant des génériques ou des biosimilaires, votre patient économise deux fois: par le prix inférieur des médicaments et par la quote-part inférieure. |
*Les produits originaux et les médicaments biologiques dont la quote-part est augmentée peuvent être consultés par chapitre IT sur www.spezialitätenliste.ch/ShowNewGenerics.aspx
Substitution des médicaments issus de la biotechnologie (art. 52a LAMal)
- Les professionnels de la santé peuvent également remplacer les médicaments issus de la biotechnologie (médicaments biologiques) par des alternatives plus économiques (biosimilaires).
Obligation d’information des patients (art. 38a al. 8 OPAS)
Les professionnels de la santé doivent informer les patients des alternatives plus économiques ayant le même principe actif; il en va de même si la quote-part du médicament est plus élevée
Obligation de documentation2
Comme auparavant, il continue d’être possible de prescrire ou de remettre un médicament plus cher pour des raisons médicales ou en cas de problèmes de livraison, sans que la quote-part augmentée ne s’applique. La justification médicale peut être par exemple une intolérance ou une efficacité insuffisante après l’essai d’au moins deux génériques ou biosimilaires. La justification doit être documentée:
- sur l’ordonnance:
- «ne pas substituer pour des raisons médicales»
- «substitution impossible en raison de difficultés de livraison»
Important: l’indication SIC n’est plus valable.
- dans le système et la facturation:
- substitution refusée par le patient
- substitution refusée par le médecin
- substitution refusée par la pharmacie
Le motif exact du refus doit être documenté. Exemple: l’impossibilité de fournir la préparation plus économique doit être documentée par une saisie d’écran de la fenêtre de commande du grossiste habituel.2
Prescrire ou délivrer proactivement des génériques et les biosimilaires élimine la charge administrative liée à l’obligation de documentation. |
1DVous trouverez des informations détaillées sur le site de l'OSPF: https://www.bag.admin.ch/bag/fr/home/gesetze-und-bewilligungen/gesetzgebung/gesetzgebung-versicherungen/gesetzgebung-krankenversicherung/kvg.html
